Gāzes siltumietilpība ir enerģijas daudzums, ko ķermenis uzņem, kad tas tiek uzkarsēts par vienu grādu. Analizēsim šī fiziskā lieluma galvenās īpašības.

Definīcijas
Gāzes īpatnējais siltums ir noteiktas vielas masas vienība. Tās mērvienības ir J/(kg·K). Siltuma daudzums, ko ķermenis uzņem, mainot tā agregācijas stāvokli, ir saistīts ne tikai ar sākotnējo un beigu stāvokli, bet arī ar pārejas metodi.

Nodaļa
Gāzu siltumietilpību dala ar vērtību, kas noteikta nemainīgā tilpumā (Cv), nemainīgā spiedienā (Cр).
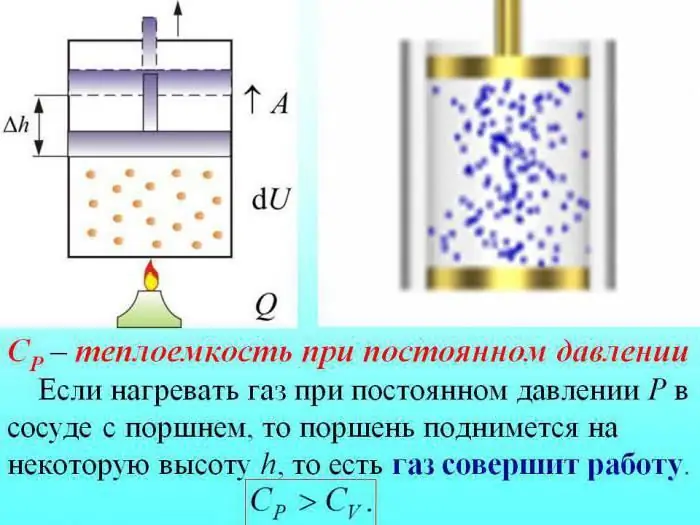
Apkures gadījumā, nemainot spiedienu, daļa siltuma tiek iztērēta, lai radītu gāzes izplešanās darbu, un daļa enerģijas tiek tērēta iekšējās enerģijas palielināšanai.
Gāzu siltumietilpību nemainīgā spiedienā nosaka siltuma daudzums, kas tiek tērēts iekšējās enerģijas palielināšanai.
Gāzes stāvoklis: funkcijas, apraksts
Ideālās gāzes siltumietilpība tiek noteikta, ņemot vērā to, ka Сp-Сv=R. Pēdējo lielumu sauc par universālo gāzes konstanti. Tā vērtība atbilst 8,314 J/(mol K).
Veicot siltumietilpības teorētiskos aprēķinus, piemēram, aprakstot saistību ar temperatūru, nepietiek tikai ar termodinamisko metožu izmantošanu, svarīgi ir bruņoties ar statiskās fizikas elementiem.
Gāzu siltumietilpība ietver dažu molekulu translācijas kustības enerģijas vidējās vērtības aprēķinu. Šāda kustība tiek summēta no molekulas rotācijas un translācijas kustības, kā arī no atomu iekšējām vibrācijām.
Statiskajā fizikā ir informācija, ka katrai rotācijas un translācijas kustības brīvības pakāpei ir gāzes daudzums, kas ir vienāds ar pusi no universālās gāzes konstantes.

Interesanti fakti
Tiek pieņemts, ka monatomiskas gāzes daļiņai ir trīs translācijas brīvības pakāpes, tāpēc gāzes īpatnējam siltumam ir trīs translācijas, divas rotācijas un viena vibrācijas brīvības pakāpes. To vienmērīgā sadalījuma likums liek īpatnējo siltumu pie nemainīga tilpuma pielīdzināt R.
Eksperimentu laikā tika konstatēts, ka divatomiskās gāzes siltumietilpība atbilst vērtībai R. Šāda teorijas un prakses neatbilstība ir izskaidrojama ar to, ka ideālas gāzes siltumietilpība ir saistīta ar kvantu. ietekmes, tāpēc, veicot aprēķinus, ir svarīgi izmantot statistiku, kas balstīta uz kvantiemmehānika.
Pamatojoties uz kvantu mehānikas pamatiem, jebkurai daļiņu sistēmai, kas svārstās vai rotē, ieskaitot gāzes molekulas, ir tikai dažas atsevišķas enerģijas vērtības.
Ja siltuma kustības enerģija sistēmā nav pietiekama, lai ierosinātu noteiktas frekvences svārstības, šādas kustības neveicina sistēmas kopējo siltuma jaudu.
Tā rezultātā "iesaldē" noteikta brīvības pakāpe, tai nav iespējams piemērot ekvipartīcijas likumu.
Gāzu siltumietilpība ir svarīga stāvokļa īpašība, no kuras ir atkarīga visas termodinamiskās sistēmas darbība.
Temperatūru, kurā līdzdalības likumu var piemērot vibrācijas vai rotācijas brīvības pakāpei, raksturo kvantu teorija, tā savieno Planka konstanti ar Bolcmaņa konstanti.

Diatomiskās gāzes
Atšķirības starp šādu gāzu rotācijas enerģijas līmeņiem ir neliels grādu skaits. Izņēmums ir ūdeņradis, kurā temperatūras vērtību nosaka simtiem grādu.
Tāpēc gāzes siltumietilpību nemainīgā spiedienā ir grūti aprakstīt ar vienmērīgas sadales likumu. Kvantu statistikā, nosakot siltumietilpību, tiek ņemts vērā, ka tās vibrācijas daļa temperatūras pazemināšanās gadījumā strauji samazinās un sasniedz nulli.
Šī parādība izskaidro faktu, ka istabas temperatūrā praktiski nav siltuma jaudas vibrācijas daļas,diatomiskā gāze, tā atbilst konstantei R.
Gāzes siltumietilpība nemainīgā tilpumā zemas temperatūras indikatoru gadījumā tiek noteikta, izmantojot kvantu statistiku. Ir Nernsta princips, ko sauc par trešo termodinamikas likumu. Pamatojoties uz tās formulu, gāzes molārā siltumietilpība samazināsies, pazeminoties temperatūrai, tiecoties uz nulli.

Cietvielu īpašības
Ja gāzu maisījuma siltumietilpību var izskaidrot, izmantojot kvantu statistiku, tad cietam agregācijas stāvoklim termisko kustību raksturo nelielas daļiņu svārstības līdzsvara stāvokļa tuvumā.
Katram atomam ir trīs vibrāciju brīvības pakāpes, tāpēc saskaņā ar līdzdalības likumu cietas vielas molāro siltumietilpību var aprēķināt kā 3nR, kur n ir atomu skaits molekulā.
Praksē šis skaitlis ir robeža, līdz kurai tiecas cieta ķermeņa siltumietilpība augstā temperatūrā.
Dažu elementu, tostarp metālu, maksimumu var iegūt parastā temperatūrā. Ja n=1, Dulong un Petit likums ir izpildīts, bet sarežģītām vielām šādu robežu sasniegt ir diezgan grūti. Tā kā robežu patiesībā nevar iegūt, notiek cietās vielas sadalīšanās vai kušana.
Kvantu teorijas vēsture
Kvantu teorijas pamatlicēji ir Einšteins un Debijs divdesmitā gadsimta sākumā. Tas ir balstīts uz atomu svārstību kustību kvantēšanu noteiktākristāls. Zemas temperatūras indikatoru gadījumā cieta ķermeņa siltumietilpība izrādās tieši proporcionāla absolūtajai vērtībai, kas ņemta kubā. Šīs attiecības tiek sauktas par Debija likumu. Kā kritērijs, kas ļauj atšķirt zemas un augstas temperatūras indikatorus, tiek ņemts to salīdzinājums ar Debī temperatūru.
Šo vērtību nosaka atoma vibrāciju spektrs ķermenī, tāpēc tā ir ļoti atkarīga no tā kristāliskās struktūras īpatnībām.
QD ir vērtība, kurai ir vairāki simti K, bet, piemēram, dimantā tā ir daudz lielāka.
Vadīšanas elektroni sniedz būtisku ieguldījumu metālu siltumietilpībā. Lai to aprēķinātu, tiek izmantota Fermi kvantu statistika. Metāla atomu elektroniskā vadītspēja ir tieši proporcionāla absolūtajai temperatūrai. Tā kā tā ir nenozīmīga vērtība, tā tiek ņemta vērā tikai temperatūrā, kas tiecas uz absolūtu nulli.
Siltuma jaudas noteikšanas metodes
Galvenā eksperimentālā metode ir kalorimetrija. Lai veiktu siltumietilpības teorētisko aprēķinu, tiek izmantota statistiskā termodinamika. Tas attiecas uz ideālu gāzi, kā arī uz kristāliskiem ķermeņiem, tiek veikts, pamatojoties uz eksperimentāliem datiem par vielas struktūru.
Empīriskās metodes ideālas gāzes siltumietilpības aprēķināšanai ir balstītas uz ideju par ķīmisko struktūru, atsevišķu atomu grupu devumu Ср.
Šķidrumiem tiek izmantotas arī metodes, kuru pamatā ir termodinamikas izmantošanacikli, kas ļauj pāriet no ideālas gāzes siltumietilpības uz šķidrumu, izmantojot iztvaikošanas procesa entalpijas temperatūras atvasinājumu.
Risinājuma gadījumā siltumietilpības aprēķins kā aditīvā funkcija nav pieļaujams, jo būtībā būtiska ir šķīduma siltumietilpības virsvērtība.
Lai to novērtētu, mums ir nepieciešama risinājumu molekulāri statistiskā teorija. Visgrūtākais ir heterogēnu sistēmu siltumietilpības noteikšana termodinamiskajā analīzē.

Secinājums
Siltuma jaudas pētījums ļauj aprēķināt ķīmiskajos reaktoros, kā arī citos ķīmiskās ražošanas aparātos notiekošo procesu enerģijas bilanci. Turklāt šī vērtība ir nepieciešama optimālu dzesēšanas šķidrumu veidu izvēlei.
Pašlaik vielu termodinamisko īpašību noteikšanas galvenā iespēja ir eksperimentāla vielu siltumietilpības noteikšana dažādiem temperatūras intervāliem - no zemām vērtībām līdz augstām vērtībām. Aprēķinot vielas entropiju un entalpiju, tiek izmantoti siltumietilpības integrāļi. Informācija par ķīmisko reaģentu siltumietilpību noteiktā temperatūras diapazonā ļauj aprēķināt procesa termisko efektu. Informācija par risinājumu siltumietilpību ļauj aprēķināt to termodinamiskos parametrus pie jebkurām temperatūras vērtībām analizētajā intervālā.
Piemēram, šķidrumu raksturo ar daļu siltuma patērēšanu, lai mainītu potenciālās enerģijas vērtībureaģējošas molekulas. Šo vērtību sauc par "konfigurācijas" siltuma jaudu, ko izmanto, lai aprakstītu risinājumus.
Ir grūti veikt pilnvērtīgus matemātiskos aprēķinus, neņemot vērā vielas termodinamiskos raksturlielumus, tās agregācijas stāvokli. Tāpēc šķidrumiem, gāzēm, cietām vielām tiek izmantots tāds raksturlielums kā īpatnējā siltumietilpība, kas ļauj raksturot vielas enerģētiskos parametrus.






