Pasaule, kurā mēs dzīvojam, ir neiedomājami skaista un pilna ar daudziem dažādiem procesiem, kas nosaka dzīves gaitu. Visus šos procesus pēta pazīstamā zinātne - fizika. Tas sniedz iespēju gūt vismaz kādu priekšstatu par Visuma izcelsmi. Šajā rakstā mēs aplūkosim tādu jēdzienu kā molekulārā kinētiskā teorija, tās vienādojumi, veidi un formulas. Tomēr, pirms pāriet pie šo jautājumu dziļākas izpētes, jums pašam ir jānoskaidro pati fizikas nozīme un tās pētāmās jomas.
Kas ir fizika?

Patiesībā šī ir ļoti plaša zinātne un, iespējams, viena no fundamentālākajām cilvēces vēsturē. Piemēram, ja viena un tā pati datorzinātne ir saistīta ar gandrīz visām cilvēka darbības jomām, vai tā ir skaitļošanas dizains vai karikatūru veidošana, tad fizika ir pati dzīve, tās sarežģīto procesu un plūsmu apraksts. Mēģināsim noskaidrot tā nozīmi, cik vien iespējams vienkāršojot izpratni.
TātadTādējādi fizika ir zinātne, kas nodarbojas ar enerģijas un matērijas izpēti, to savstarpējo saistību, daudzu mūsu plašajā visumā notiekošo procesu skaidrojumu. Vielas struktūras molekulāri kinētiskā teorija ir tikai neliels kritums teoriju un fizikas nozaru jūrā.
Enerģiju, ko šī zinātne pēta detalizēti, var attēlot dažādos veidos. Piemēram, gaismas, kustības, gravitācijas, starojuma, elektrības un daudzu citu formu veidā. Šajā rakstā aplūkosim šo formu uzbūves molekulāri kinētisko teoriju.
Matērijas izpēte sniedz priekšstatu par matērijas atomu struktūru. Starp citu, tas izriet no molekulāri kinētiskās teorijas. Zinātne par matērijas uzbūvi ļauj izprast un atrast mūsu eksistences jēgu, dzīvības rašanās iemeslus un pašu Visumu. Vēl mēģināsim pētīt vielas molekulāri kinētisko teoriju.
Pirmkārt, ir nepieciešams neliels ievads, lai pilnībā izprastu terminoloģiju un visus secinājumus.
Fizikas tēmas
Atbildot uz jautājumu, kas ir molekulāri-kinētiskā teorija, nevar nerunāt par fizikas sadaļām. Katrs no tiem attiecas uz konkrētas cilvēka dzīves jomas detalizētu izpēti un skaidrojumu. Tos klasificē šādi:
- Mehānika, kas ir sadalīta vēl divās sadaļās: kinemātikā un dinamikā.
- Statiska.
- Termodinamika.
- Molekulārā sadaļa.
- Elektrodinamika.
- Optika.
- Kvantu un atoma kodola fizika.
Parunāsim konkrēti par molekulārofizika, jo tā ir balstīta uz molekulāri-kinētisko teoriju.
Kas ir termodinamika?
Kopumā molekulārā daļa un termodinamika ir cieši saistītas fizikas nozares, kas pēta tikai makroskopisko komponentu no kopējā fizisko sistēmu skaita. Ir vērts atcerēties, ka šīs zinātnes precīzi apraksta ķermeņu un vielu iekšējo stāvokli. Piemēram, to stāvoklis karsēšanas, kristalizācijas, iztvaikošanas un kondensācijas laikā atomu līmenī. Citiem vārdiem sakot, molekulārā fizika ir zinātne par sistēmām, kas sastāv no milzīga skaita daļiņu: atomiem un molekulām.
Šīs zinātnes pētīja molekulārās kinētiskās teorijas galvenos nosacījumus.
Pat septītās klases gaitā iepazināmies ar jēdzieniem mikro un makro pasaule, sistēmas. Nebūs lieki šos terminus atsvaidzināt atmiņā.
Mikropasaule, kā mēs redzam no paša nosaukuma, sastāv no elementārdaļiņām. Citiem vārdiem sakot, šī ir mazo daļiņu pasaule. To izmēri tiek mērīti diapazonā no 10-18 m līdz 10-4 m, un to faktiskā stāvokļa laiks var sasniegt gan bezgalību, gan nesamērīgi mazi intervāli, piemēram, 10-20 s.
Makropasaule uzskata ķermeņus un sistēmas ar stabilām formām, kas sastāv no daudzām elementārdaļiņām. Šādas sistēmas ir samērīgas ar mūsu cilvēka lielumu.
Turklāt ir tāda lieta kā mega pasaule. To veido milzīgas planētas, kosmiskās galaktikas un kompleksi.
Pamatateorija
Tagad, kad esam nedaudz apkopojuši un atcerējušies fizikas pamatjēdzienus, varam pāriet tieši pie šī raksta galvenās tēmas.
Molekulāri kinētiskā teorija parādījās un pirmo reizi tika formulēta deviņpadsmitajā gadsimtā. Tās būtība slēpjas faktā, ka tajā ir sīki aprakstīta jebkuras vielas struktūra (biežāk gāzu, nevis cietu un šķidru ķermeņu struktūra), pamatojoties uz trim pamatnoteikumiem, kas apkopoti no tādu ievērojamu zinātnieku pieņēmumiem kā Roberts Huks, Īzaks. Ņūtons, Daniels Bernulli, Mihails Lomonosovs un daudzi citi.
Molekulārās kinētiskās teorijas galvenie nosacījumi izklausās šādi:
- Pilnīgi visām vielām (neatkarīgi no tā, vai tās ir šķidras, cietas vai gāzveida) ir sarežģīta struktūra, kas sastāv no mazākām daļiņām: molekulām un atomiem. Atomus dažreiz sauc par "elementārajām molekulām".
- Visas šīs elementārdaļiņas vienmēr atrodas nepārtrauktas un haotiskas kustības stāvoklī. Katrs no mums ir saskāries ar tiešu šī priekšlikuma pierādījumu, taču, visticamāk, nepiešķīra tam lielu nozīmi. Piemēram, mēs visi redzējām uz saules staru fona, ka putekļu daļiņas pastāvīgi pārvietojas haotiskā virzienā. Tas ir saistīts ar faktu, ka atomi rada savstarpējus grūdienus viens ar otru, pastāvīgi sniedzot viens otram kinētisko enerģiju. Šī parādība pirmo reizi tika pētīta 1827. gadā, un tā tika nosaukta atklājēja vārdā - "Brauna kustība".
- Visas elementārdaļiņas atrodas nepārtrauktas mijiedarbības procesā viena ar otrunoteikti spēki, kuriem ir elektrisks iezis.
Ir vērts atzīmēt, ka vēl viens piemērs, kas apraksta pozīciju numur divi, kas var attiekties arī, piemēram, uz gāzu molekulāri kinētisko teoriju, ir difūzija. Mēs ar to sastopamies ikdienas dzīvē, kā arī vairākos testos un kontrolēs, tāpēc ir svarīgi par to iegūt priekšstatu.
Vispirms apsveriet šādus piemērus:
Ārsts nejauši izlēja spirtu no kolbas uz galda. Vai varbūt jūs nometāt smaržu pudelīti, un tās izplatījās pa visu grīdu.
Kāpēc šajos divos gadījumos gan alkohola, gan smaržu smarža pēc kāda laika piepildīs visu telpu, nevis tikai vietu, kur tika izliets šo vielu saturs?
Atbilde ir vienkārša: difūzija.
Difūzija - kas tas ir? Kā tas plūst?

Šis ir process, kurā daļiņas, kas veido vienu konkrētu vielu (parasti gāzi), iekļūst citas vielas starpmolekulārajos tukšumos. Iepriekš minētajos piemēros notika sekojošais: termiskās, tas ir, nepārtrauktas un disociētas kustības dēļ spraugās starp gaisa molekulām iekrita spirta un/vai smaržu molekulas. Pakāpeniski, sadursmes ar gaisa atomiem un molekulām ietekmē, tie izplatās pa istabu. Starp citu, difūzijas intensitāte, tas ir, tās plūsmas ātrums, ir atkarīgs no difūzijā iesaistīto vielu blīvuma, kā arī no to atomu un molekulu kustības enerģijas, ko sauc par kinētisko. Jo lielāka ir kinētiskā enerģija, jo lielāks attiecīgi šo molekulu ātrums un intensitāte.
Ātrāko difūzijas procesu var saukt par difūziju gāzēs. Tas ir saistīts ar faktu, ka gāze savā sastāvā nav viendabīga, kas nozīmē, ka starpmolekulārie tukšumi gāzēs attiecīgi aizņem ievērojamu vietu, un svešas vielas atomu un molekulu nokļūšanas process tajās norit vieglāk un ātrāk..
Šķidrumos šis process ir nedaudz lēnāks. Cukura kubiņu izšķīšana tējas krūzē ir tikai piemērs cietas vielas difūzijai šķidrumā.
Bet visilgākais laiks ir difūzija ķermeņos ar cietu kristālisku struktūru. Tas ir tieši tā, jo cietvielu struktūra ir viendabīga un tai ir spēcīgs kristāliskais režģis, kura šūnās vibrē cietās vielas atomi. Piemēram, ja divu metāla stieņu virsmas ir labi notīrītas un pēc tam saskaras viena ar otru, tad pēc pietiekami ilga laika varēsim atklāt viena metāla gabalus otrā un otrādi.
Tāpat kā jebkura cita fundamentāla sadaļa, arī fizikas pamatteorija ir sadalīta atsevišķās daļās: klasifikācija, veidi, formulas, vienādojumi utt. Tādējādi mēs esam apguvuši molekulārās kinētiskās teorijas pamatus. Tas nozīmē, ka varat droši pāriet uz atsevišķu teorētisko bloku izskatīšanu.
Gāzu molekulāri-kinētiskā teorija
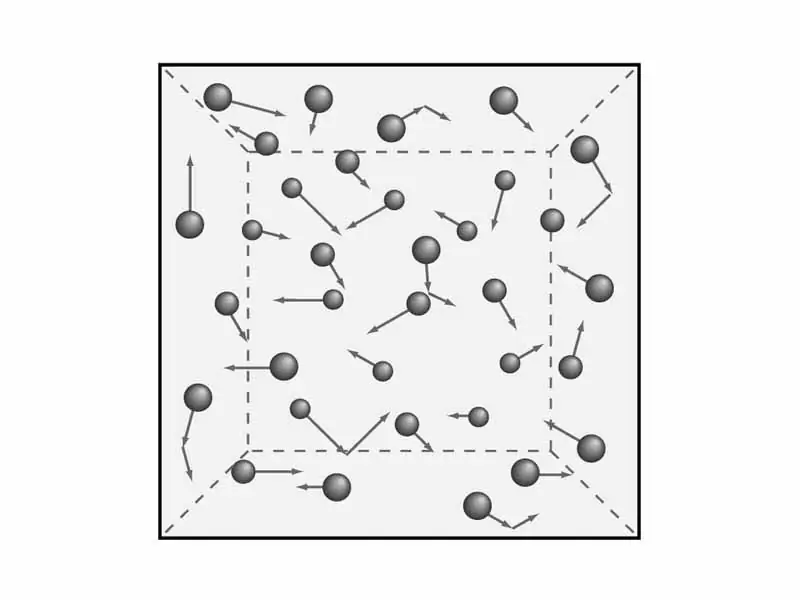
Ir nepieciešams saprast gāzes teorijas noteikumus. Kā jau teicām iepriekš, mēs apsvērsim gāzu makroskopiskās īpašības, piemēram, spiedienu un temperatūru. Tas irTas būs vajadzīgs vēlāk, lai iegūtu gāzu molekulāri kinētiskās teorijas vienādojumu. Bet matemātika - vēlāk, un tagad nodarbosimies ar teoriju un attiecīgi fiziku.
Zinātnieki ir formulējuši piecus gāzu molekulārās teorijas nosacījumus, kas palīdz izprast gāzu kinētisko modeli. Tie izklausās šādi:
- Visas gāzes sastāv no elementārdaļiņām, kurām nav noteikta izmēra, bet ir noteikta masa. Citiem vārdiem sakot, šo daļiņu tilpums ir minimāls, salīdzinot ar garumu starp tām.
- Gāzu atomiem un molekulām praktiski nav potenciālās enerģijas, attiecīgi saskaņā ar likumu visa enerģija ir vienāda ar kinētisko.
- Ar šo pozīciju jau iepazināmies agrāk - Brauna kustība. Tas nozīmē, ka gāzes daļiņas vienmēr atrodas nepārtrauktā un haotiskā kustībā.
- Absolūti visas savstarpējās gāzes daļiņu sadursmes, ko pavada ātruma un enerģijas vēstījums, ir pilnīgi elastīgas. Tas nozīmē, ka sadursmes laikā netiek zaudēta enerģija vai kinētiskā enerģija strauji lec.
- Normālos apstākļos un nemainīgā temperatūrā gandrīz visu gāzu daļiņu kustības vidējā enerģija ir vienāda.
Mēs varam pārrakstīt piekto pozīciju, izmantojot šāda veida gāzu molekulāri kinētiskās teorijas vienādojumu:
E=1/2mv^2=3/2kT, kur k ir Bolcmaņa konstante; T - temperatūra Kelvinos.
Šis vienādojums ļauj saprast saistību starp gāzes elementārdaļiņu ātrumu un to absolūto temperatūru. Attiecīgi, jo augstāks ir to absolūtaistemperatūra, jo lielāks ir to ātrums un kinētiskā enerģija.
Gāzes spiediens
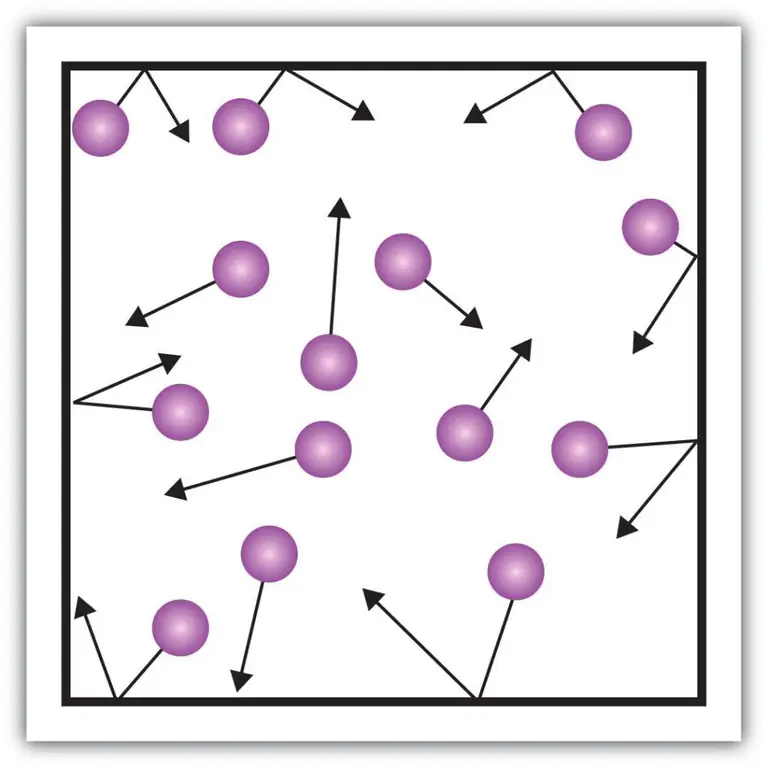
Šādus raksturlielumu makroskopiskos komponentus, piemēram, gāzu spiedienu, var izskaidrot arī, izmantojot kinētisko teoriju. Lai to izdarītu, iedomāsimies šādu piemēru.
Pieņemsim, ka kādas gāzes molekula atrodas kastē, kuras garums ir L. Izmantosim iepriekš aprakstītās gāzes teorijas nosacījumus un ņemsim vērā to, ka molekulārā sfēra kustas tikai pa x. -ass. Tādējādi varēsim novērot elastīgās sadursmes procesu ar vienu no trauka (kastes) sienām.
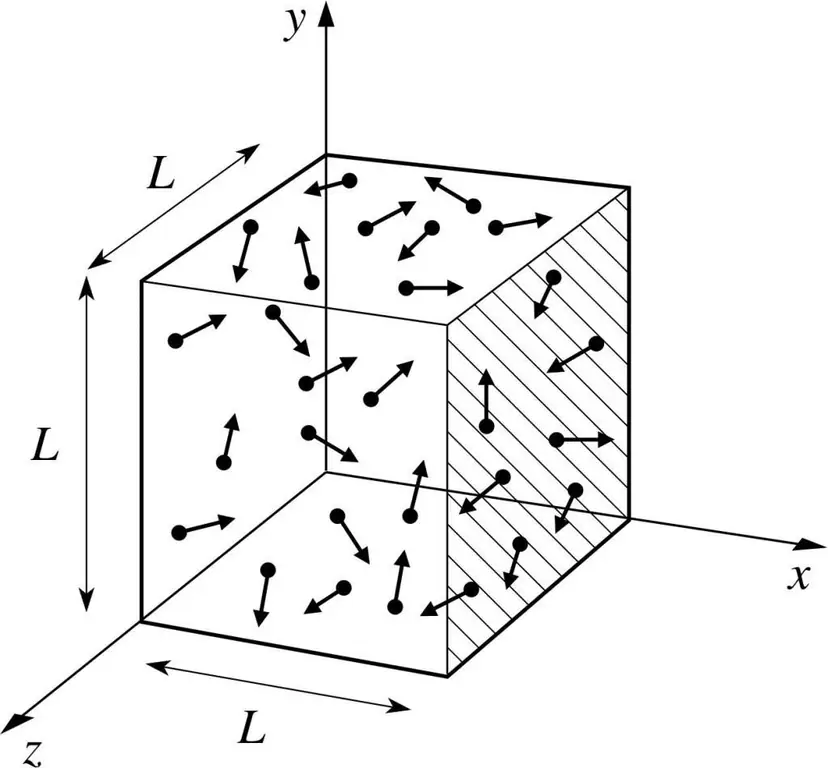
Notiekošās sadursmes impulsu, kā zināms, nosaka pēc formulas: p=mv, taču šajā gadījumā šī formula iegūs projekcijas formu: p=mv(x).
Tā kā mēs ņemam vērā tikai x ass izmēru, tas ir, x asi, kopējās impulsa izmaiņas tiks izteiktas ar formulu: mv(x) - m(-v(x))=2mv(x).
Tālāk apsveriet spēku, ko iedarbojas mūsu objekts, izmantojot Ņūtona otro likumu: F=ma=P/t.
No šīm formulām izsakām spiedienu no gāzes puses: P=F/a;
Tagad aizstāsim spēka izteiksmi iegūtajā formulā un iegūsim: P=mv(x)^2/L^3.
Pēc tam mūsu gatavo spiediena formulu var uzrakstīt N-tajam gāzes molekulu skaitam. Citiem vārdiem sakot, tas izskatīsies šādi:
P=Nmv(x)^2/V, kur v ir ātrums un V ir tilpums.
Tagad mēģināsim izcelt dažus pamatnoteikumus par gāzes spiedienu:
- Tas izpaužas caurmolekulu sadursmes ar tā objekta sienu molekulām, kurā tas atrodas.
- Spiediena lielums ir tieši proporcionāls spēkam un ātrumam, ko molekulas ietriecas trauka sieniņās.
Daži īsi secinājumi par teoriju
Pirms mēs ejam tālāk un apsveram molekulārās kinētiskās teorijas pamatvienādojumu, mēs piedāvājam jums dažus īsus secinājumus no iepriekšminētajiem punktiem un teorijas:
- Tā atomu un molekulu vidējās kustības enerģijas mērs ir absolūtā temperatūra.
- Kad divas dažādas gāzes ir vienā temperatūrā, to molekulām ir vienāda vidējā kinētiskā enerģija.
- Gāzes daļiņu enerģija ir tieši proporcionāla vidējam kvadrātveida ātrumam: E=1/2mv^2.
- Lai gan gāzes molekulām ir attiecīgi vidējā kinētiskā enerģija un vidējais ātrums, atsevišķas daļiņas pārvietojas ar dažādu ātrumu: dažas ātri, dažas lēni.
- Jo augstāka temperatūra, jo lielāks ir molekulu ātrums.
- Cik reižu mēs paaugstinām gāzes temperatūru (piemēram, divas reizes), tik reižu palielinās tās daļiņu kustības enerģija (attiecīgi dubultojas).
Pamata vienādojums un formulas

Molekulārās kinētiskās teorijas pamatvienādojums ļauj noteikt sakarību starp mikropasaules lielumiem un attiecīgi makroskopiskajiem, tas ir, izmērītajiem, daudzumiem.
Viens no vienkāršākajiem modeļiem, ko var uzskatīt molekulārajā teorijā, ir ideālais gāzes modelis.
Varētu tā teiktšis ir sava veida iedomāts modelis, ko pētīja ideālas gāzes molekulāri kinētiskā teorija, kurā:
- vienkāršākās gāzes daļiņas tiek uzskatītas par perfekti elastīgām bumbiņām, kas mijiedarbojas gan savā starpā, gan ar jebkura trauka sieniņu molekulām tikai vienā gadījumā - absolūti elastīga sadursme;
- gāzē nav pievilkšanās spēku, vai arī tos var atstāt novārtā;
- gāzes iekšējās struktūras elementus var uzskatīt par materiāliem punktiem, tas ir, to tilpumu var arī atstāt novārtā.
Ņemot vērā šādu modeli, vācu izcelsmes fiziķis Rūdolfs Klausiuss uzrakstīja formulu gāzes spiedienam, izmantojot mikro- un makroskopisko parametru attiecības. Tas izskatās šādi:
p=1/3m(0)nv^2.
Vēlāk šī formula tiks saukta par ideālas gāzes molekulāri kinētiskās teorijas pamata vienādojumu. To var pasniegt vairākos dažādos veidos. Mūsu pienākums tagad ir parādīt tādas sadaļas kā molekulārā fizika, molekulārā kinētiskā teorija un līdz ar to arī to pilnos vienādojumus un veidus. Tāpēc ir lietderīgi apsvērt citus pamatformulas variantus.
Mēs zinām, ka vidējo enerģiju, kas raksturo gāzes molekulu kustību, var atrast, izmantojot formulu: E=m(0)v^2/2.
Šajā gadījumā mēs varam aizstāt izteiksmi m(0)v^2 sākotnējā spiediena formulā ar vidējo kinētisko enerģiju. Tā rezultātā mums būs iespēja sastādīt gāzu molekulāri kinētiskās teorijas pamatvienādojumu šādā formā: p=2/3nE.
Turklāt mēs visi zinām, ka izteiksmi m(0)n var uzrakstīt kā divu koeficientu reizinājumu:
m/NN/V=m/V=ρ.
Pēc šīm manipulācijām mēs varam pārrakstīt ideālās gāzes molekulāri kinētiskās teorijas vienādojuma formulu trešajā, citā formā:
p=1/3ρv^2.
Nu, iespējams, tas ir viss, kas jums jāzina par šo tēmu. Atliek tikai sistematizēt iegūtās zināšanas īsu (un ne tik) secinājumu veidā.
Visi vispārīgie secinājumi un formulas par tēmu "Molekulāri-kinētiskā teorija"
Sāksim.
Pirmkārt:
Fizika ir dabaszinātņu kursā iekļauta fundamentāla zinātne, kas pēta matērijas un enerģijas īpašības, to uzbūvi, neorganiskās dabas modeļus.
Tajā ir iekļautas šādas sadaļas:
- mehānika (kinemātika un dinamika);
- static;
- termodinamika;
- elektrodinamika;
- molekulārā sadaļa;
- optika;
- kvantu un atoma kodola fizika.
Otrā:
Daļiņu fizika un termodinamika ir cieši saistītas nozares, kas pēta tikai makroskopisko komponentu no kopējā fizisko sistēmu skaita, tas ir, sistēmas, kas sastāv no milzīga skaita elementārdaļiņu.
Tie ir balstīti uz molekulārās kinētikas teoriju.
Trešais:
Lietas būtība ir tāda. Molekulārā kinētiskā teorija sīki apraksta vielas uzbūvi (biežāk gāzu, nevis cietvielu struktūru).un šķidrie ķermeņi), pamatojoties uz trim fundamentāliem pieņēmumiem, kas tika apkopoti no ievērojamu zinātnieku pieņēmumiem. Starp tiem: Roberts Huks, Īzaks Ņūtons, Daniels Bernulli, Mihails Lomonosovs un daudzi citi.
Ceturtais:
Trīs molekulārās kinētiskās teorijas pamatprincipi:
- Visām vielām (neatkarīgi no tā, vai tās ir šķidras, cietas vai gāzveida) ir sarežģīta struktūra, kas sastāv no mazākām daļiņām: molekulām un atomiem.
- Visas šīs vienkāršās daļiņas atrodas nepārtrauktā haotiskā kustībā. Piemērs: Brauna kustība un difūzija.
- Visas molekulas jebkuros apstākļos mijiedarbojas viena ar otru ar noteiktiem spēkiem, kuriem ir elektrisks iezis.
Katrs no šiem molekulārās kinētiskās teorijas noteikumiem ir stabils pamats matērijas struktūras izpētē.
Fifth:
Vairāki gāzes modeļa molekulārās teorijas galvenie punkti:
- Visas gāzes sastāv no elementārdaļiņām, kurām nav noteikta izmēra, bet ir noteikta masa. Citiem vārdiem sakot, šo daļiņu tilpums ir minimāls, salīdzinot ar attālumiem starp tām.
- Gāzu atomiem un molekulām praktiski nav potenciālās enerģijas, attiecīgi to kopējā enerģija ir vienāda ar kinētisko.
- Ar šo pozīciju jau iepazināmies agrāk - Brauna kustība. Tas nozīmē, ka gāzes daļiņas vienmēr atrodas nepārtrauktā un nejaušā kustībā.
- Absolūti visas savstarpējās atomu un gāzu molekulu sadursmes, ko pavada ātruma un enerģijas vēstījums, ir pilnīgi elastīgas. Tas irnozīmē, ka sadursmes laikā netiek zaudēta enerģija vai kinētiskā enerģija strauji lec.
- Normālos apstākļos un nemainīgā temperatūrā gandrīz visu gāzu vidējā kinētiskā enerģija ir vienāda.
Sestā:
Secinājumi no teorijas par gāzēm:
- Absolūtā temperatūra ir tās atomu un molekulu vidējās kinētiskās enerģijas mērs.
- Kad divas dažādas gāzes ir vienā temperatūrā, to molekulām ir vienāda vidējā kinētiskā enerģija.
- Gāzes daļiņu vidējā kinētiskā enerģija ir tieši proporcionāla vidējam kvadrātveida ātrumam: E=1/2mv^2.
- Lai gan gāzes molekulām ir attiecīgi vidējā kinētiskā enerģija un vidējais ātrums, atsevišķas daļiņas pārvietojas ar dažādu ātrumu: dažas ātri, dažas lēni.
- Jo augstāka temperatūra, jo lielāks ir molekulu ātrums.
- Cik reižu mēs paaugstinām gāzes temperatūru (piemēram, divas reizes), arī tās daļiņu vidējā kinētiskā enerģija tik reizes palielinās (attiecīgi dubultojas).
- Attiecība starp gāzes spiedienu uz trauka sienām, kurā tā atrodas, un molekulu ietekmes intensitāti uz šīm sienām ir tieši proporcionāla: jo vairāk triecienu, jo lielāks spiediens un otrādi..
Septītā:
Ideāls gāzes modelis ir modelis, kurā ir jāievēro šādi nosacījumi:
- Gāzes molekulas var un tiek uzskatītas par perfekti elastīgām bumbiņām.
- Šīs bumbiņas var mijiedarboties viena ar otru un ar jebkuras bumbas sienāmkuģis tikai vienā gadījumā - absolūti elastīga sadursme.
- Tie spēki, kas raksturo gāzes atomu un molekulu savstarpējo vilci, nepastāv vai tos var neņemt vērā.
- Atomi un molekulas tiek uzskatīti par materiāliem punktiem, tas ir, to tilpumu var arī atstāt novārtā.
Astotais:
Iesniegsim visus pamatvienādojumus un parādīsim formulas tēmā "Molekulāri-kinētiskā teorija":
p=1/3m(0)nv^2 - ideālās gāzes modeļa pamatvienādojums, ko atvasinājis vācu fiziķis Rūdolfs Klausiuss.
p=2/3nE - ideālas gāzes molekulāri kinētiskās teorijas pamatvienādojums. Atvasināts no molekulu vidējās kinētiskās enerģijas.
р=1/3ρv^2 - tas pats vienādojums, taču tiek ņemts vērā, izmantojot ideālo gāzes molekulu blīvumu un vidējo kvadrātisko ātrumu.
m(0)=M/N(a) - formula vienas molekulas masas noteikšanai, izmantojot Avogadro skaitli.
v^2=(v(1)+v(2)+v(3)+…)/N - formula molekulu vidējā kvadrātā ātruma noteikšanai, kur v(1), v(2), v (3) un tā tālāk - pirmās molekulas ātrums, otrās, trešās un tā tālāk līdz n-tajai molekulai.
n=N/V - formula molekulu koncentrācijas noteikšanai, kur N ir molekulu skaits gāzes tilpumā līdz noteiktam tilpumam V.
E=mv^2/2=3/2kT - formulas molekulu vidējās kinētiskās enerģijas noteikšanai, kur v^2 ir molekulu vidējais kvadrātiskais ātrums, k ir konstante vērtība, kas nosaukta austrieša Ludviga Bolcmaņa fizikas vārdā, un T ir gāzes temperatūra.
p=nkT - spiediena formula koncentrācijas izteiksmē, konstanteBolcmans un absolūtā temperatūra T. No tās izriet vēl viena fundamentāla formula, ko atklāja krievu zinātnieks Mendeļejevs un franču fiziķis-inženieris Klaiperons:
pV=m/MRT, kur R=kN(a) ir universālā konstante gāzēm.
Tagad parādīsim konstantes dažādiem izoprocesiem: izobāriskajiem, izohoriskajiem, izotermiskajiem un adiabātiskajiem.
pV/T=const - veic, kad gāzes masa un sastāvs ir nemainīgi.
рV=const - ja arī temperatūra ir nemainīga.
V/T=const - ja gāzes spiediens ir nemainīgs.
p/T=const - ja skaļums ir nemainīgs.
Varbūt tas ir viss, kas jums jāzina par šo tēmu.
Šodien mēs ienirt tādā zinātnes jomā kā teorētiskā fizika, tās vairākas sadaļas un bloki. Sīkāk mēs pieskārāmies tādai fizikas jomai kā fundamentālā molekulārā fizika un termodinamika, proti, molekulāri-kinētiskā teorija, kas, šķiet, sākotnējā pētījumā nesagādā nekādas grūtības, bet patiesībā tai ir daudz nepilnību.. Tas paplašina mūsu izpratni par ideālās gāzes modeli, kuru mēs arī detalizēti pētījām. Turklāt ir vērts atzīmēt, ka mēs iepazināmies arī ar molekulārās teorijas pamatvienādojumiem to dažādajās variācijās, kā arī izskatījām visas nepieciešamākās formulas noteiktu nezināmu lielumu atrašanai par šo tēmu. Tas būs īpaši noderīgi, gatavojoties rakstīt. jebkādus testus, eksāmenus un ieskaites, vai paplašināt vispārējo skatījumu un zināšanas par fiziku.
Ceram, ka šis raksts jums bija noderīgs, un jūs no tā esat ieguvis tikai pašu nepieciešamāko informāciju, nostiprinot savas zināšanas tādos termodinamikas pīlāros kā molekulārās kinētiskās teorijas pamatnosacījumi.






