Viens no svarīgākajiem jautājumiem termodinamisko sistēmu izpētē fizikā ir jautājums par to, vai šī sistēma var veikt kādu noderīgu darbu. Ar darba jēdzienu cieši saistīts ir iekšējās enerģijas jēdziens. Šajā rakstā mēs apsvērsim, kāda ir ideālās gāzes iekšējā enerģija, un sniegsim formulas tās aprēķināšanai.
Ideāla gāze
Par gāzi, kā agregācijas stāvokli, kam ārējā iedarbībā nav elastības spēka un kā rezultātā tā nesaglabā apjomu un formu, zina katrs skolēns. Ideālas gāzes jēdziens daudziem joprojām ir nesaprotams un neskaidrs. Paskaidrosim.
Ideāla gāze ir jebkura gāze, kas atbilst šādiem diviem svarīgiem nosacījumiem:
- Daļiņām, kas to veido, nav izmēra. Viņiem ir izmērs, taču tas ir tik mazs, salīdzinot ar attālumiem starp tiem, ka to var ignorēt visos matemātiskajos aprēķinos.
- Daļiņas mijiedarbojas viena ar otru, izmantojot van der Vāla spēkus vai spēkuscita daba. Faktiski visās reālajās gāzēs šāda mijiedarbība pastāv, taču tās enerģija ir niecīga salīdzinājumā ar kinētisko daļiņu vidējo enerģiju.
Aprakstītos nosacījumus izpilda gandrīz visas reālās gāzes, kuru temperatūra ir virs 300 K un spiedieni nepārsniedz vienu atmosfēru. Pārāk augsta spiediena un zemas temperatūras gadījumā tiek novērota gāzu novirze no ideālās uzvedības. Šajā gadījumā runā par īstām gāzēm. Tos apraksta van der Vālsa vienādojums.
Ideālas gāzes iekšējās enerģijas jēdziens
Saskaņā ar definīciju sistēmas iekšējā enerģija ir šajā sistēmā ietvertās kinētiskās un potenciālās enerģijas summa. Ja šī koncepcija tiek piemērota ideālai gāzei, potenciālā sastāvdaļa ir jāizmet. Patiešām, tā kā ideālās gāzes daļiņas savstarpēji mijiedarbojas, var uzskatīt, ka tās brīvi pārvietojas absolūtā vakuumā. Lai no pētāmās sistēmas iegūtu vienu daļiņu, nav nepieciešams strādāt pret iekšējiem mijiedarbības spēkiem, jo šie spēki nepastāv.
Tādējādi ideālas gāzes iekšējā enerģija vienmēr sakrīt ar tās kinētisko enerģiju. Pēdējo savukārt unikāli nosaka sistēmas daļiņu molārā masa, to skaits, kā arī vidējais translācijas un rotācijas kustības ātrums. Kustības ātrums ir atkarīgs no temperatūras. Temperatūras paaugstināšanās izraisa iekšējās enerģijas pieaugumu un otrādi.
Formula priekšiekšējā enerģija
Ideālās gāzes sistēmas iekšējo enerģiju apzīmē ar burtu U. Saskaņā ar termodinamiku to definē kā starpību starp sistēmas entalpiju H un spiediena un tilpuma reizinājumu, tas ir:
U=H - pV.
Augšējā rindkopā mēs noskaidrojām, ka U vērtība atbilst kopējai kinētiskajai enerģijai Ekvisu gāzes daļiņu:
U=Ek.
No statistikas mehānikas ideālās gāzes molekulāri kinētiskās teorijas (MKT) ietvaros izriet, ka vienas daļiņas Ek1 vidējā kinētiskā enerģija ir vienāda ar šāda vērtība:
Ek1=z/2kBT.
Šeit kB un T - Bolcmana konstante un temperatūra, z - brīvības pakāpju skaits. Sistēmas kopējo kinētisko enerģiju Ek var iegūt, reizinot Ek1 ar daļiņu skaitu N sistēmā:
Ek=NEk1=z/2NkBT.
Tādējādi mēs esam ieguvuši ideālās gāzes iekšējās enerģijas formulu, kas uzrakstīta vispārīgā formā absolūtās temperatūras un daļiņu skaita izteiksmē slēgtā sistēmā:
U=z/2NkBT.
Monatomiskā un daudzatomiskā gāze
Raksta iepriekšējā rindkopā uzrakstītā U formula ir neērta tās praktiskajai lietošanai, jo ir grūti noteikt daļiņu N skaitu. Taču, ja ņemam vērā vielas daudzuma definīciju n, tad šo izteiksmi var pārrakstīt ērtākā formā:
n=N/NA; R=NAkB=8, 314 J/(molK);
U=z/2nR T.
Brīvības pakāpju skaits z ir atkarīgs no gāzi veidojošo daļiņu ģeometrijas. Tādējādi monoatomiskajai gāzei z=3, jo atoms var pārvietoties neatkarīgi tikai trīs telpas virzienos. Ja gāze ir diatomiska, tad z=5, jo trim translācijas brīvības pakāpēm tiek pievienotas vēl divas rotācijas brīvības pakāpes. Visbeidzot, jebkurai citai daudzatomu gāzei z=6 (3 translācijas un 3 rotācijas brīvības pakāpes). Paturot to prātā, mēs varam ierakstīt ideālas vienatomiskas, divatomiskas un daudzatomiskas gāzes iekšējās enerģijas formulas šādā formā:
U1=3/2nRT;
U2=5/2nRT;
U≧3=3nRT.
Uzdevuma piemērs iekšējās enerģijas noteikšanai
100 litru balonā ir tīrs ūdeņradis ar spiedienu 3 atmosfēras. Pieņemot, ka ūdeņradis noteiktos apstākļos ir ideāla gāze, ir jānosaka, kāda ir tā iekšējā enerģija.

Iepriekš minētās U formulas satur vielas daudzumu un gāzes temperatūru. Problēmas stāvoklī par šiem daudzumiem nav teikts pilnīgi nekas. Lai atrisinātu problēmu, ir jāatgādina universālais Klapeirona-Mendeļejeva vienādojums. Tā izskats ir parādīts attēlā.
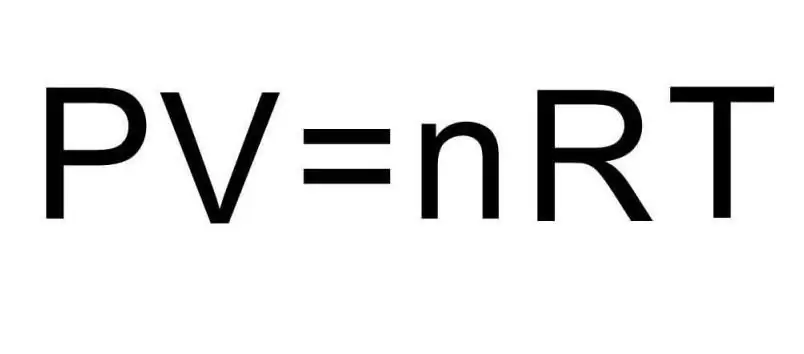
Tā kā ūdeņradis H2 ir divatomu molekula, iekšējās enerģijas formula ir:
UH2=5/2nRT.
Salīdzinot abas izteiksmes, mēs nonākam pie galīgās problēmas risināšanas formulas:
UH2=5/2PV.
Atliek konvertēt spiediena un tilpuma vienības no stāvokļa uz SI vienību sistēmu, aizstāt atbilstošās vērtības formulā UH2 un iegūt atbilde: UH2 ≈ 76 kJ.






