Termodinamika ir svarīga fizikas nozare. Varam droši teikt, ka tās sasniegumi ir noveduši pie tehnoloģiju laikmeta rašanās un lielā mērā ir noteikuši cilvēces vēstures gaitu pēdējo 300 gadu laikā. Rakstā apskatīts pirmais, otrais un trešais termodinamikas likums un to pielietojums praksē.
Kas ir termodinamika?
Pirms formulēt termodinamikas likumus, izdomāsim, ko dara šī fizikas sadaļa.
Vārdam "termodinamika" ir grieķu izcelsme un tas nozīmē "kustība karstuma dēļ". Tas ir, šī fizikas nozare nodarbojas ar jebkādu procesu izpēti, kā rezultātā siltumenerģija tiek pārvērsta mehāniskā kustībā un otrādi.
Terodinamikas pamatlikumi tika formulēti 19. gadsimta vidū. Zinātne par "kustību un siltumu" aplūko visas sistēmas uzvedību kopumā, pētot tās makroskopisko parametru - temperatūras, spiediena un tilpuma - izmaiņas un nepievēršot uzmanību tās mikroskopiskajai struktūrai. Turklāt pirmajam no tiem ir būtiska loma likumu formulēšanātermodinamika fizikā. Interesanti atzīmēt, ka tie ir iegūti tikai no eksperimentāliem novērojumiem.
Termodinamiskās sistēmas jēdziens

Tas nozīmē jebkuru atomu, molekulu vai citu elementu grupu, kas tiek uzskatīta par veselu. Visi trīs likumi ir formulēti tā sauktajai termodinamiskajai sistēmai. Piemēri: Zemes atmosfēra, jebkurš dzīvs organisms, gāzu maisījums iekšdedzes dzinējā utt.
Visas termodinamikas sistēmas pieder vienam no trim veidiem:
- Atvērts. Viņi apmainās gan ar siltumu, gan vielu ar vidi. Piemēram, ja ēdiens tiek gatavots katlā uz atklātas uguns, tad tas ir spilgts atvērtas sistēmas piemērs, jo katls saņem enerģiju no ārējās vides (uguns), savukārt pats izstaro enerģiju siltuma veidā, un no tā arī iztvaiko ūdens (vielmaiņa).
- Slēgts. Šādās sistēmās nenotiek vielu apmaiņa ar vidi, lai gan notiek enerģijas apmaiņa. Atgriežoties pie iepriekšējā gadījuma: ja tējkannu nosedz ar vāku, var iegūt slēgtu sistēmu.
- Izolēts. Šī ir sava veida termodinamiskās sistēmas, kas neapmainās ar vielu vai enerģiju ar apkārtējo telpu. Piemērs varētu būt termoss ar karstu tēju.
Termodinamiskā temperatūra

Šis jēdziens nozīmē apkārtējos ķermeņus veidojošo daļiņu kinētisko enerģiju, kas atspoguļo ātrumunejauša daļiņu kustība. Jo lielāks tas ir, jo augstāka temperatūra. Attiecīgi, samazinot sistēmas kinētisko enerģiju, mēs to atdzesējam.
Šis jēdziens nozīmē apkārtējos ķermeņus veidojošo daļiņu kinētisko enerģiju, kas atspoguļo daļiņu haotiskās kustības ātrumu. Jo lielāks tas ir, jo augstāka temperatūra. Attiecīgi, samazinot sistēmas kinētisko enerģiju, mēs to atdzesējam.
Termodinamisko temperatūru izsaka SI (Starptautiskā vienību sistēma) Kelvinos (par godu britu zinātniekam Viljamam Kelvinam, kurš pirmo reizi ierosināja šo skalu). Izprast pirmo, otro un trešo termodinamikas likumu nav iespējams bez temperatūras definīcijas.
Viena grāda dalījums pēc Kelvina skalas atbilst arī vienam grādam pēc Celsija. Konvertēšana starp šīm vienībām tiek veikta pēc formulas: TK =TC + 273, 15, kur TK un TC - temperatūras attiecīgi kelvinos un Celsija grādos.
Kelvina skalas īpatnība ir tāda, ka tai nav negatīvu vērtību. Nulle tajā (TC=-273, 15 oC) atbilst stāvoklim, kad sistēmas daļiņu termiskās kustības pilnībā nav., šķiet, ka tie ir "iesaldēti".
Enerģijas saglabāšana un 1. termodinamikas likums

1824. gadā franču inženieris un fiziķis Nikolass Leonards Sadi Karno izteica drosmīgu ieteikumu, kas ne tikai noveda pie fizikas attīstības, bet arī kļuva par nozīmīgu soli tehnoloģiju uzlabošanā. Viņavar formulēt šādi: "Enerģiju nevar radīt vai iznīcināt, to var tikai pārnest no viena stāvokļa citā."
Patiesībā Sadi Karno frāze postulē enerģijas nezūdamības likumu, kas bija termodinamikas 1. likuma pamatā: "Kad sistēma saņem enerģiju no ārpuses, tā pārvērš to citās formās, kas ir termiski un mehāniski."
1.likuma matemātiskā formula ir uzrakstīta šādi:
Q=ΔU + A, šeit Q ir siltuma daudzums, ko vide pārnes sistēmai, ΔU ir šīs sistēmas iekšējās enerģijas izmaiņas, A ir ideāls mehāniskais darbs.
Adiabātiskie procesi
Labs to piemērs ir gaisa masu kustība pa kalnu nogāzēm. Šādas masas ir milzīgas (kilometri vai vairāk), un gaiss ir lielisks siltumizolators. Norādītās īpašības ļauj uzskatīt par adiabātiskiem jebkādus procesus ar gaisa masām, kas notiek īsā laikā. Kad gaiss paceļas kalna nogāzē, tā spiediens pazeminās, tas izplešas, tas ir, veic mehānisku darbu un rezultātā atdziest. Gluži pretēji, gaisa masas kustību uz leju pavada spiediena paaugstināšanās tajā, tā saspiežas un līdz ar to kļūst ļoti karsta.
Terodinamikas likuma piemērošanu, kas tika apspriesta iepriekšējā apakšvirsrakstā, visvieglāk var demonstrēt, izmantojot adiabātiskā procesa piemēru.
Saskaņā ar definīciju, tās rezultātā nenotiek enerģijas apmaiņa arvide, tas ir, augstāk esošajā vienādojumā Q=0. Tas noved pie šādas izteiksmes: ΔU=-A. Mīnusa zīme šeit nozīmē, ka sistēma veic mehānisku darbu, samazinot savu iekšējo enerģiju. Jāatgādina, ka iekšējā enerģija ir tieši atkarīga no sistēmas temperatūras.
Termisko procesu virziens
Šajā izdevumā ir apskatīts termodinamikas 2. likums. Noteikti visi pamanīja, ka, saskaroties ar diviem priekšmetiem ar atšķirīgu temperatūru, aukstais vienmēr uzkarsīs, bet karstais atdziest. Ņemiet vērā, ka apgrieztais process var notikt pirmā termodinamikas likuma ietvaros, taču tas nekad netiek īstenots praksē.
Šī procesa (un visu Visumā zināmo procesu) neatgriezeniskuma iemesls ir sistēmas pāreja uz daudz ticamāku stāvokli. Aplūkotajā piemērā ar divu dažādu temperatūru ķermeņu saskari visticamākais būs tāds stāvoklis, kurā visām sistēmas daļiņām būs vienāda kinētiskā enerģija.
Otro termodinamikas likumu var formulēt šādi: "Siltums nekad nevar spontāni pāriet no auksta ķermeņa uz karstu." Ja mēs ieviešam entropijas jēdzienu kā nekārtības mēru, tad to var attēlot šādi: "Jebkurš termodinamiskais process norisinās ar entropijas pieaugumu".
Siltumdzinējs

Ar šo terminu saprot sistēmu, kas, pateicoties tai ārējās enerģijas padevei, var veikt mehāniskus darbus. Pirmkārtsiltuma dzinēji bija tvaika dzinēji un tika izgudroti 17. gadsimta beigās.
Otrajam termodinamikas likumam ir izšķiroša loma to efektivitātes noteikšanā. Sadi Carnot arī konstatēja, ka šīs ierīces maksimālā efektivitāte ir: Efektivitāte=(T2 - T1)/T2, šeit T2 un T1 ir sildītāja un ledusskapja temperatūra. Mehānisku darbu var veikt tikai tad, ja notiek siltuma plūsma no karsta ķermeņa uz aukstu, un šo plūsmu nevar 100% pārvērst lietderīgā enerģijā.
Zemāk redzamajā attēlā parādīts siltumdzinēja darbības princips (Qabs - siltums pārnests uz mašīnu, Qced - siltuma zudumi, W - lietderīgs darbs, P un V - spiediens un gāzes tilpums virzulī).
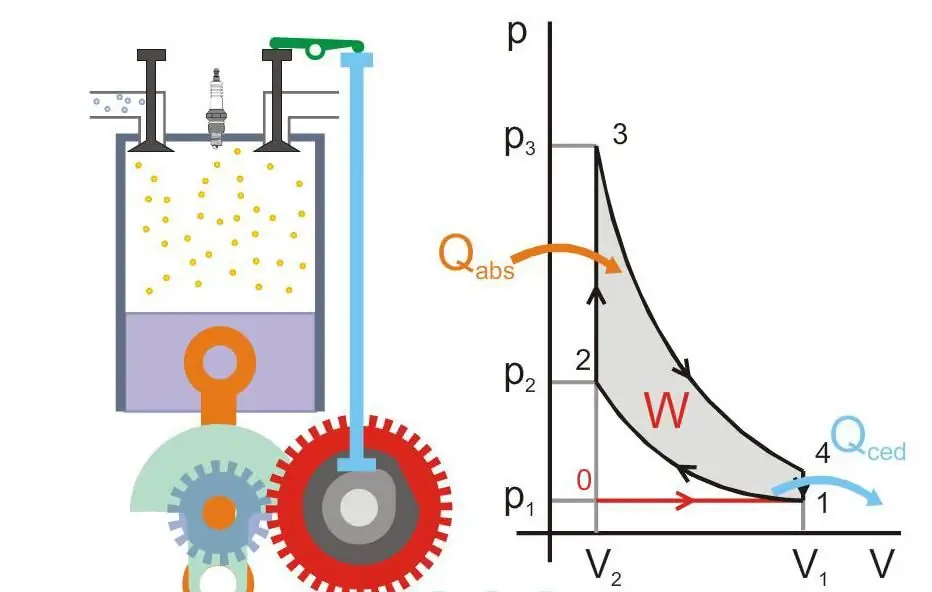
Absolūtā nulle un Nernsta postulāts
Visbeidzot, pāriesim pie trešā termodinamikas likuma. To sauc arī par Nernsta postulātu (tā vācu fiziķa vārds, kurš to pirmo reizi formulēja 20. gadsimta sākumā). Likums saka: "Absolūto nulli nevar sasniegt ar ierobežotu procesu skaitu." Tas ir, nav iespējams nekādā veidā pilnībā "iesaldēt" vielas molekulas un atomus. Iemesls tam ir pastāvīgā siltuma apmaiņa ar vidi.

Viens noderīgs secinājums, kas izdarīts no trešā termodinamikas likuma, ir tāds, ka entropija samazinās, virzoties uz absolūto nulli. Tas nozīmē, ka sistēma tiecas organizēties pati. Šis fakts varizmantojiet, piemēram, lai paramagnētus atdzesētu pārnestu feromagnētiskā stāvoklī.
Interesanti atzīmēt, ka līdz šim zemākā sasniegtā temperatūra ir 5·10−10 K (2003, MIT laboratorija, ASV).






