Adiabātiskā pāreja starp diviem stāvokļiem gāzēs nav viens no izoprocesiem, tomēr tai ir liela nozīme ne tikai dažādos tehnoloģiskajos procesos, bet arī dabā. Šajā rakstā mēs apsvērsim, kas ir šis process, kā arī sniegsim adiabātiskos vienādojumus ideālai gāzei.
Ideāla gāze īsumā
Ideāla gāze ir tāda gāze, kurā starp daļiņām nav mijiedarbības un to izmēri ir vienādi ar nulli. Dabā, protams, simtprocentīgi ideālu gāzu nav, jo tās visas sastāv no molekulām un izmēra atomiem, kas vienmēr mijiedarbojas savā starpā vismaz ar van der Vāla spēku palīdzību. Tomēr aprakstītais modelis bieži tiek veikts ar pietiekamu precizitāti, lai atrisinātu praktiskas problēmas daudzām reālām gāzēm.
Ideālās gāzes galvenais vienādojums ir Klapeirona-Mendeļejeva likums. Tas ir uzrakstīts šādā formā:
PV=nRT.
Šis vienādojums nosaka tiešu proporcionalitāti starp produktuspiediens P uz tilpumu V un vielas daudzums n uz absolūto temperatūru T. R vērtība ir gāzes konstante, kas spēlē proporcionalitātes faktora lomu.
Kas ir adiabātiskais process?
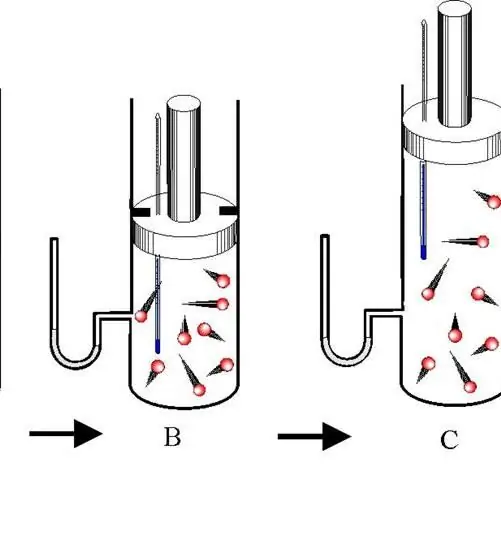
Adiabātiskais process ir pāreja starp gāzes sistēmas stāvokļiem, kuros nenotiek enerģijas apmaiņa ar vidi. Šajā gadījumā mainās visas trīs sistēmas termodinamiskās īpašības (P, V, T), un vielas n daudzums paliek nemainīgs.
Atšķiriet adiabātisko izplešanos un kontrakciju. Abi procesi notiek tikai sistēmas iekšējās enerģijas dēļ. Tātad izplešanās rezultātā sistēmas spiediens un jo īpaši temperatūra krasi pazeminās. Un otrādi, adiabātiskā saspiešana rada pozitīvu temperatūras un spiediena lēcienu.
Lai novērstu siltuma apmaiņu starp vidi un sistēmu, pēdējai jābūt ar siltumizolētām sienām. Turklāt procesa laika saīsināšana ievērojami samazina siltuma plūsmu uz sistēmu un no tās.
Puasona vienādojumi adiabātiskajam procesam

Pirmais termodinamikas likums ir uzrakstīts šādi:
Q=ΔU + A.
Citiem vārdiem sakot, sistēmai nodotais siltums Q tiek izmantots, lai sistēma veiktu darbu A un palielinātu tās iekšējo enerģiju ΔU. Lai uzrakstītu adiabātisko vienādojumu, jāliek Q=0, kas atbilst pētāmā procesa definīcijai. Mēs iegūstam:
ΔU=-A.
Ar izohoriskuprocess ideālā gāzē, viss siltums tiek novirzīts iekšējās enerģijas palielināšanai. Šis fakts ļauj mums uzrakstīt vienādību:
ΔU=CVΔT.
Kur CV ir izohoriskā siltuma jauda. Darbu A savukārt aprēķina šādi:
A=PdV.
Kur dV ir nelielas skaļuma izmaiņas.
Papildus Klapeirona-Mendeļejeva vienādojumam ideālajai gāzei ir spēkā šāds vienādojums:
CP- CV=R.
Kur CP ir izobāriskā siltumietilpība, kas vienmēr ir lielāka par izohorisko, jo ņem vērā gāzes zudumus izplešanās rezultātā.
Analizējot iepriekš uzrakstītos vienādojumus un integrējot temperatūru un tilpumu, mēs nonākam pie šāda adiabātiskā vienādojuma:
TVγ-1=const.
Šeit γ ir adiabātiskais indekss. Tas ir vienāds ar izobariskās siltumietilpības attiecību pret izohorisko. Šo vienādību sauc par Puasona vienādojumu adiabātiskajam procesam. Piemērojot Klapeirona-Mendeļejeva likumu, jūs varat uzrakstīt vēl divas līdzīgas izteiksmes, tikai izmantojot parametrus P-T un P-V:
TPγ/(γ-1)=const;
PVγ=const.
Adiabātisko grafiku var norādīt dažādās asīs. Zemāk tas ir parādīts P-V asīs.
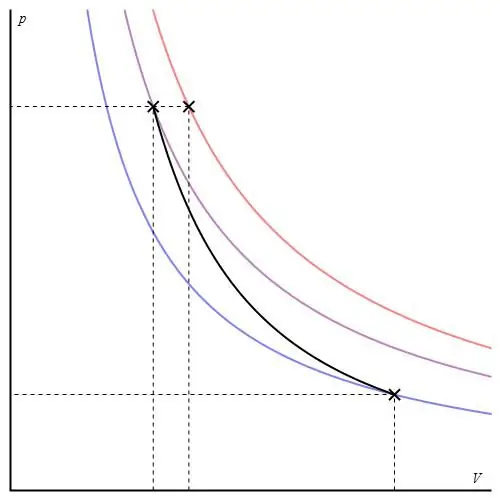
Krāsainās līnijas grafikā atbilst izotermām, melnā līkne ir adiabāts. Kā redzams, adiabāts uzvedas asāk nekā jebkura izoterma. Šo faktu ir viegli izskaidrot: izotermai spiediens mainās atpakaļproporcionāls tilpumam, bet izobātam spiediens mainās ātrāk, jo eksponents ir γ>1 jebkurai gāzes sistēmai.
Problēmas piemērs
Dabā, kalnu apvidos, gaisa masai virzoties augšup pa nogāzi, tās spiediens pazeminās, palielinās apjoms un atdziest. Šis adiabātiskais process pazemina rasas punktu un rada šķidrus un cietus nokrišņus.

Ir ierosināts atrisināt šādu problēmu: gaisa masas celšanas procesā pa kalna nogāzi spiediens pazeminājās par 30%, salīdzinot ar spiedienu pakājē. Kāda būtu tā temperatūra, ja tā pēdā būtu 25 oC?
Lai atrisinātu problēmu, izmantojiet šādu adiabātisko vienādojumu:
TPγ/(γ-1)=konst.
Labāk to rakstīt šādā formā:
T2/T1=(P2/P 1)(γ-1)/γ.
Ja P1 ņem par 1 atmosfēru, tad P2 būs vienāds ar 0,7 atmosfērām. Gaisa adiabātiskais indekss ir 1,4, jo to var uzskatīt par diatomisku ideālu gāzi. Temperatūras vērtība T1 ir 298,15 K. Aizstājot visus šos skaitļus iepriekš minētajā izteiksmē, mēs iegūstam T2=269,26 K, kas atbilst - 3, 9 oC.






